导读:
这篇深度文章拆解了一家瑞士制药巨头如何建起最后一个伟大的企业创新实验室,并分析为什么这种模式可能再也行不通。
Alex Kesin|撰文
莫喻枫|翻译
2002 年,马克·菲什曼(Mark Fishman,中文名费思明)走进了美国剑桥市的一栋玻璃大楼,肩负着一项不同寻常的任务:把瑞士制药公司诺华(Novartis)打造成为全球最卓越的治疗药物研究机构。
这位哈佛大学的心脏病学家一生都在研究斑马鱼心脏,并教授医学生。至少表面看来,他是最不适合担任这份工作的人。他没有任何制药行业经验,也没有商业背景。然而,诺华创始人丹尼尔·魏思乐(Daniel Vasella),这位由医生转型为 CEO 、曾在 1996 年主导了汽巴-嘉基(Ciba-Geigy)与山德士(Sandoz)的合并,从而成立诺华的人,如今却把数十亿美元交到菲什曼手中,希望他重振公司内部的药物研发体系。
菲什曼到任的时机并不乐观。当时,制药行业的研发产出比正以每九年减一半的速度下降。2000 年代初,一美元研发投入所能产出的药物,仅仅是 1950 年代的一小部分。整个制药行业正在调整策略:与其在内部发现新药,不如通过收购获得创新药物。辉瑞(Pfizer)四处收购公司,默克(Merck)削减研究预算,即便是以深厚研究传统著称的罗氏(Roche),也开始转向外部合作。行业共识几乎是一致的:内部研发的时代已经结束。
但菲什曼并不这么认为。
然而出人意料的是,在随后的十四年里,这项看似不合常理的任命不仅结出了成果,还逐渐打破了现代制药管理的诸多原则。诺华生物医学研究所(NIBR)在菲什曼任期内,公司 65% 的新药批准来自内部研发。其中许多药物为公司带来了数百亿美元的收入。这在当时是一件近乎幻想的事情。这一研究体系延续到了 2016 年,随后被诺华拆解。
这是一个关于一位学者型心脏病学家和一位 CEO 的故事:他们证明,出于纯粹好奇心的研究方式,也能做出达到制药工业顶尖水准的成果。同时,这也是一个关于为何即使取得这样的成功,也依然无法让一个研究机构免于残酷市场力量冲击的故事。
从曾经的繁荣到“青铜时代崩溃”
当丹尼尔·魏思乐在 2001 年宣布诺华将建立行业规模最大的企业研究组织时,时机再糟糕不过。
20 世纪 90 年代末,制药安全性问题引发了行业信心危机,危机一直延续到了 21 世纪初。1997 年至 2001 年间,共有 12 种处方药(约占所有上市药物的 5%)被撤出市场。其中大多数是出于安全性问题。
例如,曾经风靡一时的减肥药组合“fen-phen” (注:由芬特明和芬氟拉明组成的联合减肥药物)被发现会损害心脏瓣膜,从而终止了第一波减肥药热潮。
随后,在 1999 年 9 月,18 岁的杰西·盖尔辛格(Jesse Gelsinger)在一次基因治疗临床试验中死亡,成为首位被公开确认因实验性基因治疗而死亡的患者。这一事件极大震动了监管机构,以至于当时被高度看好的基因治疗领域几乎一夜之间崩溃,其影响持续了数十年。
尽管这些事件已经非常严重,但仍然比不上 Vioxx 事件。2004 年,当默克撤回其重磅止痛药 Vioxx 时,估计已有 2000 万美国人服用过这种药物。研究表明,该药物与 8.8 万例心脏病发作和 3.8 万例死亡有关。随后,美国国会举行听证会,并爆发了数千起诉讼案件。这导致业内所称的 “监管棘轮效应”(regulatory ratchet effect):一次药品安全失败会导致监管标准进一步收紧,而这些标准几乎不会再放松。
这些失败改变了研发的优先级。负责研发的科学家们变得不再愿意做大胆的尝试。许多公司设立额外的安全检查点并更早地终止高风险项目,风险承担逐渐让位于风险规避。
与此同时,由于大多数常见疾病已经有廉价且有效的仿制药治疗,很多公司不得不进入更困难和充满未知的疾病领域,而这些领域的失败率本身就更高。
面对这一局面,整个行业采取了意料之中但影响深远的策略:合并与外包。
药企们并没有修复自己的研发体系,而是通过合并来扩大规模,或者干脆放弃内部药物研发。相反,它们转向由风险投资支持的生物技术公司,让它们承担早期研究的风险;大型制药公司则主要负责昂贵但成功率更高的 III 期临床试验。
到魏思乐决定聘请菲什曼时,这种谨慎的模式已成为行业标准。
糖果工厂政变
马克·菲什曼成为诺华研发负责人,其实是一个颇为奇特的选择。
这位哈佛医学院教授发表过许多心脏遗传学论文,但在学术界外很少有人读过。尽管他没有受过商业训练、没有制药行业经验,也没有管理数十亿美元研发业务的明显资历,但他有一样东西:真正的科学好奇心。当行业老手们能说出无数理由证明一些宏大的计划行不通时,菲什曼并没有预设它们“做不到”。他的学术背景使他习惯从生物学机制而不是市场细分的角度思考问题,也更重视科学问题本身,而非利润率。
那么,为什么是菲什曼?
魏思乐之所以挖走他,很大程度上因为自己也是医学背景。当时,他是唯一一位领导大型制药公司的医生。许多商业背景的高管把人类基因组计划(Human Genome Project)带来的海量新靶点视为一种需要通过成本控制来管理的挑战,而魏思乐却把它看作千载难逢的科学机遇,需要采取完全相反的策略。
他赌的是:只有一种以人才为核心、深度投入的研究模式,才能把基因组革命转化为突破性的药物。而这种模式需要耐心资本 (Patient capital),也需要相信科学,而不是只看财务报表。
聘请菲什曼只是诺华押注“好奇心驱动科学”的一部分。
2002年,魏思乐还决定把诺华的全球研究总部从瑞士巴塞尔迁往美国马萨诸塞州剑桥市。此前从未有欧洲制药巨头如此彻底地离开自己的大本营。魏思乐认为:真正的突破性创新需要沉浸在更丰富的生物技术生态系统中,即使这意味着切断传统商业关系。
菲什曼的新研究所设在肯德尔广场(Kendall Square)、靠近麻省理工学院的一座旧厂房。那曾是新英格兰糖果公司 的工厂。曾经生产数百万块粉状糖果薄片的生产线,如今被 900 名新招聘的科学家取代,他们在那里搭建起实验台。
魏思乐说:“我们必须去人才所在的地方。美国剑桥市拥有世界上其他地方都找不到的科学人才资源。”
在这里,魏思乐要求菲什曼建立一种研究文化:吸收产业界与学术界各自最好的部分。
诺华生物医学研究所将独立于诺华的市场部门运作,研究优先级不会由销售团队决定,同时项目的选择标准是它们是否有潜力“改变医学实践”,而不取决于商业前景。
当被问到研究战略时,菲什曼画出了一个 2×2 矩阵:一条轴是“未满足的医疗需求”,另一条轴是“机制理解”。最理想的位置在右上角:为迫切需要治疗的患者开发具有清晰生物学机制的药物。
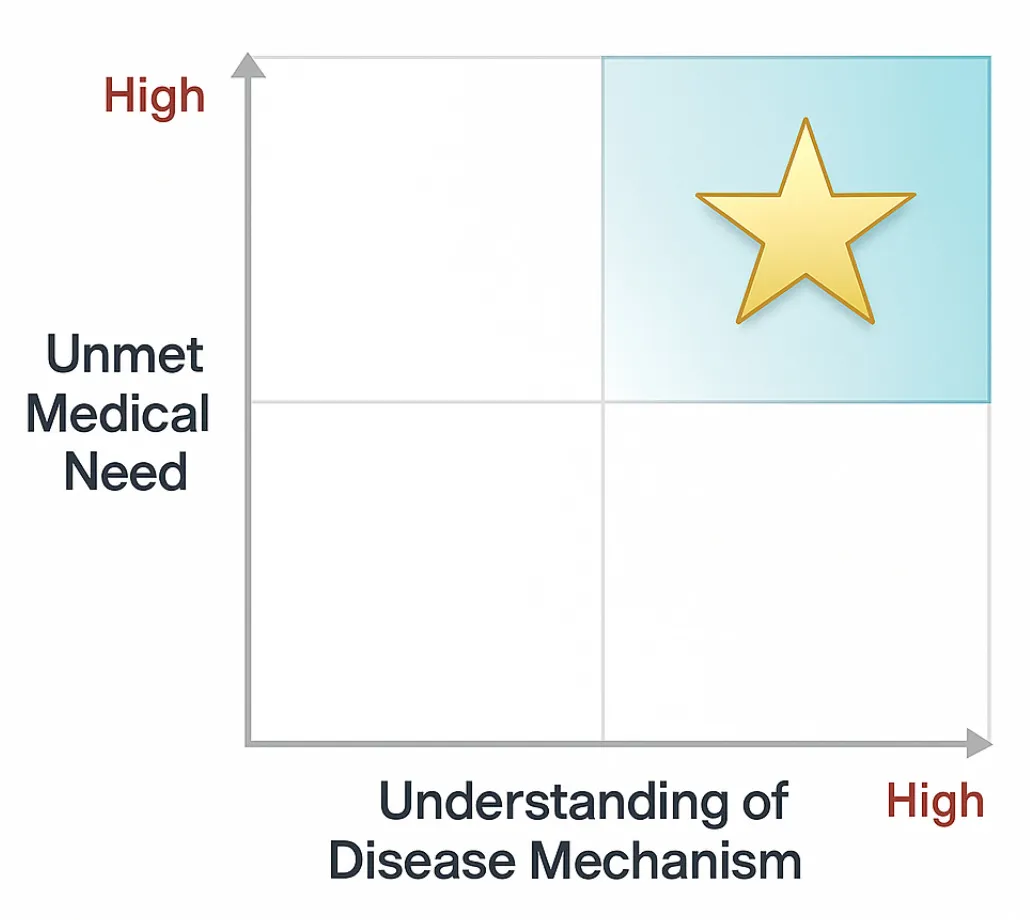
菲什曼的研发模型
“图表上没有的是什么?” 菲什曼说道,“是钱……我们是唯一一个不根据市场潜力来评估项目的团队。”
诺华生物医学研究所明确拒绝通过追踪效率指标、计算财务回报、以及砍掉无法承诺巨额利润的项目来进行财务简化管理的做法。当诺华开始拒绝现代制药管理的基本教条时,这一结构性基础被证明至关重要。
诺华生物医学研究所的四大“异端”
随后,在菲什曼的领导下,诺华生物医学研究所(NIBR)的四大组织原则凝练而出,这些原则甚至违背了整个行业从过往危机中吸取的所有教训。每一个原则,或者更应该说是“异端”,都针对了危机时代制药管理的一种特定失败模式。当它们组合在一起时,形成了一套可以持续产生突破性创新的系统。
第一个异端是在极端表型患者中快速完成概念验证。你可以称之为聪明的药物开发,尽管它的运作更像是一个科学上的“作弊码”。事实证明,那些绝望的、罕见的病例,是生物学最诚实的见证者,在他们身上能以惊人的速度验证机制。
菲什曼团队开发卡纳单抗(canakinumab)的策略很好地体现了这种激进理念。卡纳单抗是一种靶向 IL-1β 的抗体,这是一种关键的炎症信号分子。如果按照传统思路,研发目标会是类风湿性关节炎。
治疗类风湿性关节炎是一个诱人的目标:130 万患者,成熟的市场,有成为“重磅药物”的清晰路径。任何制药高管都能在睡梦中规划出这个战略,而且大多数人也确实会这么做。
然而,菲什曼的团队却转向了 Muckle-Wells 综合征,这种病发现于 1962 年,在全球范围内仅发现 400 名患者。这个人数在商业上几乎可以忽略不计。
但这些患者提供了一些无价的东西:对 IL-1β 重要性的纯粹测试。
他们每天的发烧来自一个遗传突变,该突变会持续让体内产生大量 IL-1β。如果在这些患者体内阻断 IL-1β,药物作用将会非常明显。
于是诺华对这些患者进行了临床试验。第一位患者的发烧在一天内消退。随后,所有患者都几乎立刻产生反应——持续了几十年的每日发烧突然消失,就像有人终于在一栋从童年起就闷热不堪的房子里找到了恒温器。
一次给药,24小时,概念验证完成。这种快速验证为后续研究奠定了基础。研究人员随后将同一机制扩展到多个炎症疾病,包括全身型幼年特发性关节炎、痛风和动脉粥样硬化。
最终的验证来自 CANTOS 试验。这是一项纳入 1 万名既往心血管疾病患者的大型心血管预防研究。研究进行四年后,菲什曼接到来自公司高层的电话:“这次最好能成功。” 结果果然成功了:心梗、中风或心血管死亡的综合风险下降 15%。然后出现了一个出人意料的结果:肺癌发生率下降了67%。
一个最初在 400 名罕见病患者身上、用 24 小时完成概念验证的研究,最终揭示了影响数百万人疾病的炎症机制。
第二条异端顺理成章地产生:按生物学通路组织研究,而不是按疾病市场分类。
制药行业通常按照市场领域组织研究,例如心血管、肿瘤学、神经学,NIBR 则围绕生物学本身组织研究,追踪那些连接不同疾病的古老分子通路。
一个典型案例是芬戈莫德(fingolimod,又名FTY720) 的研发历程。这种药物最初来源于一种真菌 Isaria sinclairii 的天然产物类似物。
其机制既优雅又反直觉:这种药物与淋巴细胞(免疫系统的步兵)相互作用,并迫使它们被隔离在淋巴结中。被困在淋巴结中的淋巴细胞无法进入血液循环,也就无法进入组织造成损伤。
最初,这种药物的开发目标是肾移植。目标是通过暂时抑制免疫系统来防止器官排斥。但结果并不理想。
肾脏项目失败了,并不是因为机制错了,而是因为疾病选择不对。移植患者本身已经接受了非常强的免疫抑制治疗,因此芬戈莫德的机制很难显示额外优势。
大多数制药公司会在此时放弃这一机制。但诺华生物医学研究所选择提出一个完全不同的问题:还有哪些疾病是由异常免疫细胞引起的?
答案来自一个意想不到的方向:多发性硬化(Multiple Sclerosis)。在这种疾病中,T 细胞会穿过血脑屏障并攻击髓鞘,从而导致神经系统逐渐受损。如果芬戈莫德能阻止免疫细胞在血液中循环,它是否也能阻止免疫血包进入大脑?
答案是:可以。
当 Gilenya(芬戈莫德的商品名)于 2010 年获得 FDA 批准时,它成为首个口服多发性硬化治疗药物。一个失败的移植药物最终变成了年销售额 30 亿美元的重磅药物。这一成功验证了诺华生物医学研究所的理念:疾病研究应由生物学通路驱动,而不是由市场分类驱动。
第三个异端挑战了行业本身与学术界的关系。大多数制药公司把大学视为潜在竞争者,或是与现实脱节的“象牙塔”,通常只维持较为疏远的技术授权关系。
而 NIBR 采取了完全不同的策略。
他们不仅聘请教授,还重建了制药公司与知识创造体系之间的关系。当竞争对手把研究封闭在企业内部时,诺华生物医学研究所鼓励其研究人员大量发表论文、在会议上做报告,并维持深入的大学合作。
诺华生物医学研究所能够如此自信地从生物学洞察走向临床验证,部分原因在于其不寻常的组织结构:负责药物发现的研发人员,会护送他们的分子通过首次人体试验。
与那种将筛选出的化合物从研究部门“扔过墙”给开发部门负责的传统制药模式不同,NIBR 从第一天起就让转化医学方向的医生参与研究团队。这些医生兼科学家会一直参与到早期临床试验阶段,从而保证关键生物学洞见不会在过程中丢失。
例如在卡纳单抗的临床试验中,理解其分子机制的研究人员,正是设计临床试验方案的人。NIBR 的研发科学家在 Nature、Cell、Science 等顶级期刊发表论文的数量,与顶尖大学相当。
这种开放文化甚至成为招聘工具,因为它证明:加入诺华并不意味着放弃科学理想。
这种开放性延伸到了最非常规的研究领域,比如衰老生物学(gerontology)。大多数竞争对手避开衰老研究,认为它太基础、太冒险、周期太长。然而,NIBR 却看到了它解锁多个治疗领域的潜力。虽然听起来不性感,但每个人都会变老。
这种拥抱被忽视机会的哲学,在另一个领域被证明至关重要。宾夕法尼亚大学的免疫学家卡尔·朱恩(Carl June)正在开创CAR-T细胞疗法——一种通过基因工程改造患者免疫细胞来杀死癌细胞的革命性技术。诺华和宾大没有进行标准的许可交易,而是建立了一个深度的共同开发联盟,并在宾大校园内建立了诺华-宾大先进细胞治疗中心。
最终,这一合作产生了 Kymriah ——世界上首个获批的细胞疗法。
当耐药突变不可避免地出现时,学术界与产业界的团队会合作解析其机制,并开发下一代治疗策略。这种与学术界的深度整合,消除了通常存在于药物发现与开发之间的“死亡之谷”。正因为那些真正理解相关生物学机制的科学家始终参与临床方案的设计,NIBR 才能确保关键的科学洞见不会在转化过程中丢失。
NIBR的第四个也是最后一个异端是:不要因为某个研究领域已经被大量研究过或曾经失败而放弃它。
当竞争对手专注于在可预测的开发周期内进行从头(de novo)药物发现时,NIBR 选择在几十年前的研究基础上继续推进。
一个典型例子是 Entresto(LCZ696)。科学家们发现,身体通过涉及血管紧张素(angiotensin)的激素级联反应来控制循环,这是一种会收缩血管并升高压力的应激激素。ACE 抑制剂在1980年代问世,能改善心衰患者预后,但仍有一半患者在五年内死亡。后来出现了一种新策略:阻断一种名为脑啡肽酶(neprilysin)的酶,以提升利钠肽(一种保护心脏的激素,能帮助肾脏排出盐分),同时阻断有害的血管紧张素通路。
但由于这种药物也提高了一种可能导致危及生命的喉咙肿胀的分子缓激肽(bradykinin)的水平,FDA在 2002 年拒绝了它。
NIBR在这次失败中看到了机会。他们没有彻底放弃双重方法,而是花了五年时间围绕它进行重新设计。奥马曲拉的喉咙肿胀问题源于它阻断血管紧张素的方式,因此NIBR将他们的脑啡肽酶抑制剂与缬沙坦(valsartan,他们已经获批的降压药)配对。这消除了缓激肽问题,同时保留了双重益处。
由此产生的复方药物 LCZ696,后来被命名为 Entresto 面临着最艰难的基准测试。它必须直接与依那普利(enalapril,金标准的ACE抑制剂)正面较量。与依那普利相比,LCZ696 将主要复合终点降低了20%。全因死亡率下降了16%。但时间线却很长。到 2015 年 7 月 Entresto 获批时,距离配对的降压药缬沙坦的首次合成已经过去了 28 年。到 2024 年,它已经成长为一个价值 78 亿美元的产品线。
当竞争对手在每个项目上都从头开始时,NIBR 的第四个“异端”迫使他们将自己的整个研究历史视为累积的资本。他们认识到,突破性药物是通过耐心且刻意地建立在数十年的生物学理解之上的。
诺华生物医学研究所的成绩单
NIBR 创造了令人瞩目的成果:65% 的诺华新药来自内部研发(相比之下,辉瑞为 20%),其 16.7% 的 FDA 批准率在大型研发公司中排名第四。四种 NIBR 药物——Gilenya、Cosentyx、Entresto 和 Affinitor——创造了1080 亿美元的终身销售额,推动诺华在全球制药公司排名中从 2004 年的第 7 位攀升至 2014 年全球第 2 位。
当 NIBR 在不断开辟全新的生物学领域时,那些奉行更保守路线的竞争对手们,回报却在不断下降。阿斯利康(AstraZeneca)采用显性的净现值(NPV)门槛,并削减了超过 40% 的研发管线。GSK 则设立了“终止委员会(kill committees)”,根据投资回报率(ROI)来终止超过 35% 的发现项目。这种以财务回报为核心的做法,结果正如经济学理论所预期:创新变成了小修小补,决策也越来越趋于保守。
换个角度来看:NIBR 四款药(Gilenya、Cosentyx、Entresto 和 Affinitor)的总收入,可与成熟制药公司一整年的营收相媲美,如莫德纳(180亿美元)、再生元(120亿美元)或渤健(109亿美元)。魏思乐当年投入到一间剑桥糖果工厂的 2.5 亿美元赌注,最终创造了与多个进入 500 强的制药公司营收规模相当的成果。
NIBR 似乎解决了制药研发中的一个根本悖论,即如何在一家大型组织内部,持续地产生突破性的创新。它提出的四项原则,看起来为实现这一点提供了一套可以复制的方法,去做到竞争对手认为不可能的事情。在十多年时间里,这一模式的成功似乎牢不可破。
但推动整个行业走向“外包化”的市场力量依旧存在,并在每一次季度财报电话会上愈发强烈。来自投资者的财务压力不断升级。
NIBR 的结局证明:即便是最成功的创新模型,也无法在以短期回报为优化目标的系统中永续生存。
当这套体系难以为继
2016 年 3 月,马克·菲什曼在担任 NIBR 主席十三年后卸任,由哈佛化学生物学家杰伊·布拉德纳(Jay Bradner)接任。菲什曼的离开,留下了一个无法填补的哲学真空。他不仅是 NIBR 的创始人,更是它的精神象征,是在商业压力下坚持“生物学优先”的守护者。
但财务现实变得越来越无法忽视。
NIBR 的年度运营成本膨胀到 40 亿美元,这笔钱足以支持多个国家级科研基金会。当初看似前瞻性的投资,如今被股东视为浪费,因为他们要求季度回报。一份今年早些时候出炉的麦肯锡分析甚至提出:采取“外部创新”模式的公司,其单位投资的股东回报是维持内部研发公司的 3–8 倍。
在黄金时代,NIBR 曾扩展至全球,在上海、新加坡和加州设立专门研究中心。但从 2016 年开始,这些研究网络开始收缩,诺华关闭了一些基地并整合运营结构。诺华的新闻稿中反复强调“关键规模”和“运营效率”,但这些不过是企业惯用的委婉说法,实际上意味着业务布局过于分散。与此同时,关键研究人员也在持续流失。许多资深研发科学家带着在机构多年积累的知识离开,其中不少投身于剑桥市的生物技术公司。
甚至 NIBR 最成功的药物也面临越来越激烈的竞争。曾经领先的银屑病药物 Cosentyx 受到新药挑战,例如礼来的 ixekizumab、UCB 的 bimekizumab,它们的疗效更佳。与此同时,曾经开创口服多发性硬化治疗的 Gilenya,也逐渐被百时美施贵宝的 Zeposia 和强生的 Ponvory 取代,因为这些药免除了 Gilenya 的麻烦的心脏监测要求。
曾经的旗舰产品,如今却像被鱼雷不断击中的战舰,一点点被拆解。所谓的产品生命周期管理,也逐渐变成了被动的补救。
在菲什曼时代,项目评估主要基于生物学合理性和机制清晰度。但随着财务压力的增大,这些标准逐渐加入了市场规模、竞争格局和峰值销售预测。项目要想存活,必须承诺巨额营收。
但讽刺的是:对“重磅药物”市场的追逐,反而让 NIBR 偏离了当初促成其早期成功的“极端表型”策略,结果接连遭遇失败。
心衰激素 Serelaxin 在 III 期失败,损失 2 亿美元;哮喘药 Fevipiprant 在投入多年后于 2019 年夭折;最具毁灭性的是 CNP520,一款阿尔茨海默药物,它不仅失败,还似乎加速了认知退化;即使是 Ilaris,尽管 CANTOS 成功,但仍被 FDA 拒绝批准心血管适应证。到 2019 年,NIBR 以前所未有的速度关闭临床项目,因为仅一年内就有 21 个候选药物夭折。
当来自默克的资深制药主管菲奥娜·马歇尔(Fiona Marshall)在 2022 年末接替布拉德纳时,她接手的,仿佛是一个从高处跌落的瑞士手表,外表仍在,但组织内部原本精密的结构已经被严重打乱。
马歇尔上任后的第一项举动颇具象征意味,也耐人寻味:原本复数形式的“Novartis Institutes of Biomedical Research” 被改为单数“Novartis Biomedical Research”。这一处改变,像一枚“语言上的中子弹”,瞬间抹去了近二十年来积累的研究自主权。
在 2023 年 STAT Future Summit 上,她表示 NIBR 将专注于“有望产生商业成功药物的项目……我们希望实现这种‘一致性(alignment)’。”
“一致性” 一词变得至关重要。某项目是否拥有明确的、近期的商业路径,将决定其能否获得批准。换句话说,现在的研究项目只有在开发与市场团队提前看到盈利与获批路径时,才能启动。这意味着菲什曼的“生物学优先”的信条被商业考量所取代。而像 Entresto 这种在早期看来毫无商业前景、但最终极其成功的项目,在这种新体系下根本不会存活。
她在另一场采访中进一步强调:新的 NIBR 不会再探索科学家“觉得很酷”的发现,而是要“与开发战略保持一致”。这意味着 NIBR 原有的文化正式终结,制药行业也完全被财务压力重塑。
内部研发:濒危物种
制药公司发现了一件比发现新药更赚钱的事情:干脆不去发现新药。
2016 至 2020 年间,全球十四家最大的制药公司在股票回购和分红上花费了 5770 亿美元,而用于研发的投入为 5210 亿美元,这意味着它们在金融上的投入,比真正的技术研发多出了 560 亿美元。到 2024 年 7 月,甚至连诺华的新任 CEO 万思瀚(Vas Narasimhan)也坦率地对投资者表示:“我们更愿意把资金用于回购公司股票……目前仍有 100 亿美元的回购计划在进行中。”
这种做法可以理解为制药公司在吃掉明天的种子粮。每一美元从研发中转移出去,就意味着一种本可能被发现的疗法不会出现,一条可能被探索的生物学线索不会被追寻,也意味着一类患者的需求得不到满足。
行业对此的回应,是把创新外包出去。
自 2018 年以来,新兴生物医药公司主导了 73% 的晚期临床项目,并贡献了 72% 的新 FDA 批准药物。大型制药公司实际上越来越像是授权和市场运营机构,而不再是药物发现的引擎。
然而,这种策略或许聪明过头了。如果“购买创新”真的如此高效,那么企业为什么还需要内部研发?因为内部研发提供了一些无法替代的东西,例如内部的知识经验积累(哪些靶点曾因毒性失败?)、科学判断(如果内部没有真正做研究的人,商务开发团队如何判断一家小型生物技术公司的数据是否可靠?),以及长期视角(生物技术公司必须在融资周期结束前实现退出,而不管这是否符合药物研发的最佳时间节奏)。
如果没有像 NIBR 这样的机构,整个行业就会越来越集中于已被验证的机制,而不是突破性的发现。制药公司逐渐失去研究能力,生物技术公司则优化策略以尽快被收购,而真正的创新反而变得在经济上更具风险。
事实上,我们所看到的是:制药创新本身需要“低效率”。
它需要资助十个项目,才能换来一个成功;它需要科学家去追逐那些直觉性的想法,而这些想法往往会被 MBA 出身的项目经理当场否决;也需要那种耐心、好奇、甚至常常显得“浪费”的研究。这种研究在资本市场看来不受欢迎,但却是人类真正需要的。
剑桥那座玻璃大楼依然矗立着,如今更像是一座被刻意遗忘的纪念碑。那些曾经创造不可能的人已经四散而去:有人进入生物技术公司,有人回到学术机构,也有人进入咨询行业。他们带走了整个行业似乎已经决定忘记的知识与经验。
这个故事的教训,并不是 NIBR 的模式失败了;而是即便被证明有效的创新模式,也难以在季度业绩压力下长期存活。菲什曼提出的四项“异端”原则创造了数百亿美元的疗法收入,它们今天依然和二十年前一样有效。但整个行业选择了可预测的回报,而不是不确定的突破;选择了季度业绩,而非长期影响。
随着 NIBR 这样的机构消失的,是解决那些我们尚未理解的问题的能力。每一个没有“生物学优先”研究的季度,都意味着一整代原本可能出现的疗法就此消失。
NIBR 的这场二十年实验已经结束。我们记录了每一次成功,分析了每一次突破,然后又一步步拆解了自己学到的一切。问题并不在于我们是否从中学到了什么,而在于我们是否愿意忽视这些经验,安于那种“管理衰退”的平庸状态。
选择,依然在我们手中。
而患者,仍在等待。
原文链接:https://www.alexkesin.com/p/the-day-novartis-chose-discovery
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 